May 8, 2020
Bob Bickler
フラッシュクロマトグラフィーは、有機化学者のワークフローのスタンダードな工程です。生成された副産物や過剰な試薬のほとんどを除去するために、ほとんどの反応ステップの後に行われます。
全フラッシュクロマトグラフィーアプリケーションの 90%には、化学者は未結合シリカゲルを使用しています。残りの 10%は、逆相(C18)、アミノシリカゲル(NH2)、または他の吸着剤を含む代替固相を使用しています。
これまで シリカゲル と 逆相 の使用について頻繁に議論してきましたが、アミノシリカゲルについては、それを使う理由や最適な場所についてはほとんど話したことがありませんでした。各メディアの化学的性質に注目してみましょう。
シリカゲル
シリカゲルは通常、珪酸ナトリウムを原料とし、表面積、気孔率、および粒径などの特定の特性が得られるように反応条件が設計されています。シリカゲルカラムには、球状と粒状(不規則)の両方の粒子形状があります。球状シリカゲルは、前述したように、特定のパラメータのセットに合わせて製造されます。粒状シリカゲルもまた、特定の仕様に合わせて製造されますが、粒子径は大きくなります。このシリカゲルは、その後、粉砕されてより小さな粒子となり、様々な粒子径またはメッシュ範囲に分離されます。
シリカゲルは様々なシラノール(Si-OH)官能基を様々な比率で含んでいます。シリカゲルカラムに含まれるシラノールは酸性(ブレンステッド酸)であり、有機塩基を精製しようとすると、塩基性化合物が酸性シリカに付着し、除去・分離が困難になるという問題が生じます。このような場合には、極性の高い溶媒、例えば、塩基を添加したメタノールなどを使用すると、目的の結果を得ることができます。しかし、このような精製方法は、開発に時間がかかり、必ずしもうまくいくとは限りません。
逆相
逆相メディアは、シリカと疎水性試薬(例えばオクタデシルシラン)を結合させたものです。このメディアは、うまく結合していれば、水性溶媒系を使用して有機塩基を分離・溶出することができます。しかし、溶出バンド幅を減らして分離能を向上させるために、pH 調整剤や緩衝剤が一般的に使用されていますが、それでも必要な結果が得られない場合があります。
アミノシリカゲル
アミノプロピル基などでシラノール基に修飾したアミノシリカゲルは、シリカカラムや塩基性有機溶媒に加え、緩衝液や pH 調整された水系溶媒システムを使用する逆相カラムに代わるものです。
アミノシリカゲルは、表面官能基のアミノ基によって土台となるシリカの酸性度が低下し、図1 に示すように塩基性化合物のクロマトグラフィーに適した化学環境を作り出します。
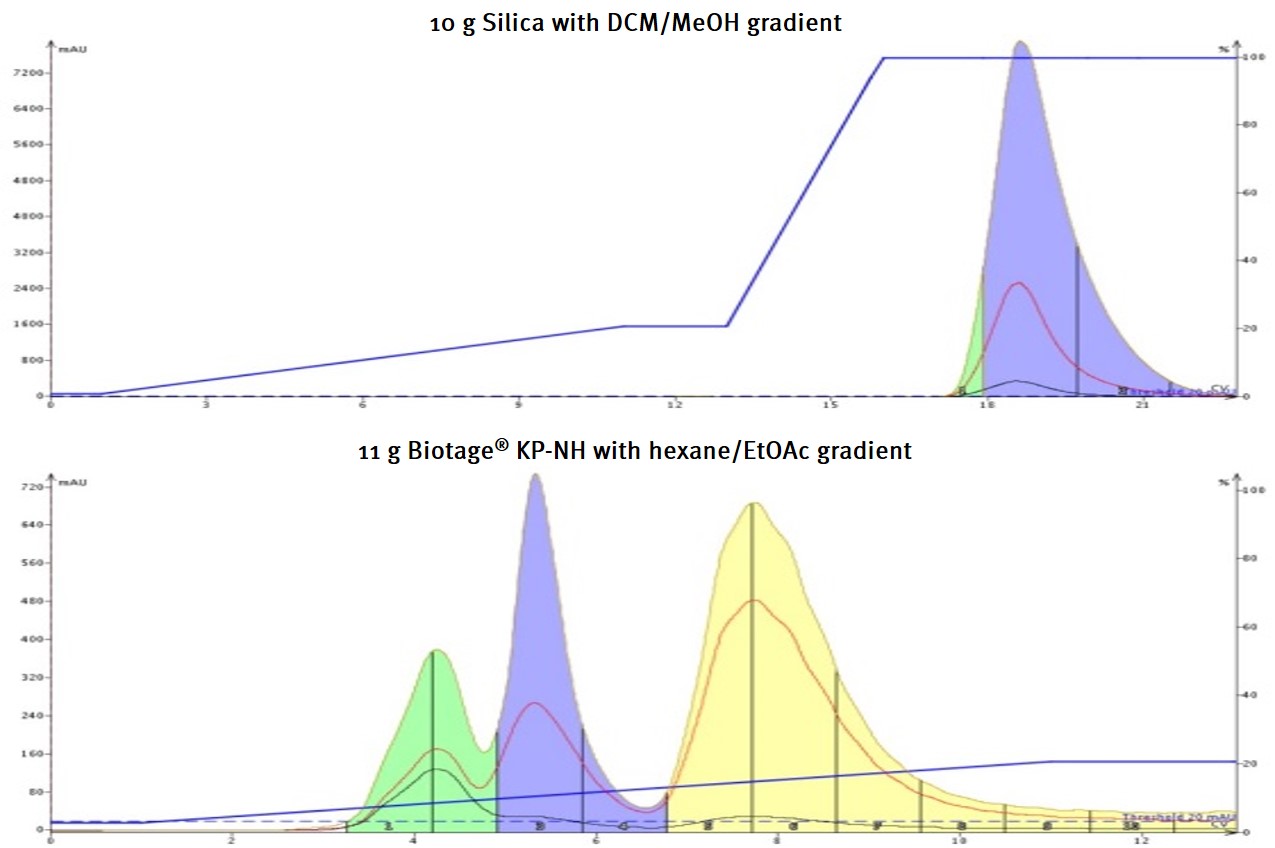
図 1. .3 つの塩基性三環式アミン(すべて pKa >9)のフラッシュクロマトグラフィー分離。上 – DCM-MeOH グラジエントを用いたシリカゲルカラムでは化合物の分離に失敗し、溶出に 100%メタノールを必要とした。下部-アミノシリカゲルカラムは、ヘキサン/酢酸エチルのグラジエントを用いて 3 つの化合物を分離した。
本実施例では、3つの三環式アミン(すべて強塩基性)の混合物を、シリカゲルカラムとアミノシリカゲルカラム(Biotage® Sfär KP-Amino)に注入しました。化合物をまずはシリカ ゲルTLC プレートと KP-アミノシリカゲルTLC プレート上で異なる溶媒を用いて分離しました。
シリカゲル-80% DCM + 20% MeOH
KP-NH – 90%ヘキサン+10%酢酸エチル
両方のプレートで化合物はすべて分離しますが (データは示されていません)、シリカゲルカラムを 100% メタノールで洗浄するまで、化合物はシリカゲルカラムから溶出せず、分離できませんでした。しかし、KP-アミノシリカゲルカラムでは、ヘキサンと酢酸エチルを混ぜるだけで、3 つの塩基性三環式アミンを簡単に分離し、溶出させることができました。
そのような中、ランドルフ・メーコン大学[1]のお客様から、図 2 に示すメソ-テトラ-(p-ブロモフェニル)ポルフィリン[2]というポルフィリン化合物を合成したので、その精製を手伝ってほしいと協力の依頼がありました。
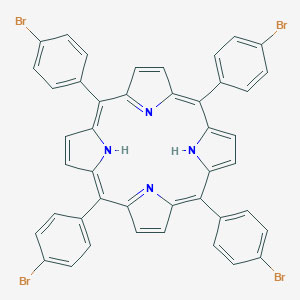
図 2. メソ-テトラ-(p-ブロモフェニル)ポルフィリンの構造。
反応混合物を精製するために、シリカゲルカラムと逆相カラムの両方を試しました。逆相カラムを使用しても分離は達成されませんでしたが、順相シリカゲルカラムでヘキサン-酢酸エチルのグラジエントをかけると、良好ではありますが、優れた分離は得られませんでした(図 3)。
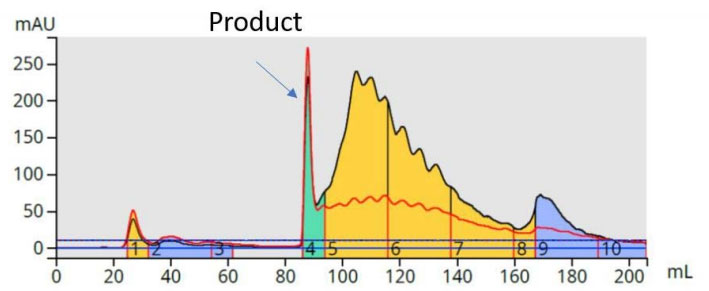
図 3. メソ-テトラ-(p-ブロモフェニル)ポルフィリン反応混合物をヘキサン-酢酸エチルグラジエントを用いてシリカカラムで精製すると、生成物とその反応副生成物の不純物が部分的に分離される。
この結果に満足していなかった私は、その後、Biotage® Sfär Amino カラムを用いて、同じくヘキサン-酢酸エチルグラジエントを試してみたところ、この組み合わせは非常にうまくいきました[3](図 4)。
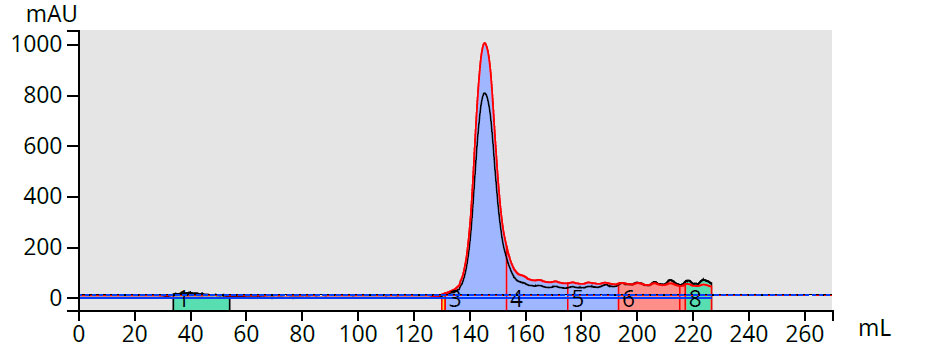
図 4. メソ-テトラ-(p-ブロモフェニル)ポルフィリン反応混合物のアミン結合カラム精製により、生成物と溶出しなかった不純物が完全に分離される。
では、なぜアミノシリカゲルカラムが最も効果があったのでしょうか?ポルフィリンの構造には 4 つのアミンが含まれており、それらがシリカの酸性シラノールに引き寄せられているのです。生成物とその副生成物の両方がシリカに親和性があるため、分離は可能ですが、不完全になります。しかし、アミノシリカゲルカラムは副生成物を選択的に結合させるので、生成物を分離して純粋な紫色の画分として溶出させることができます。
フラッシュクロマトグラフィーの詳細についてご興味のある方は、下記ボタンからホワイトペーパーをご覧ください。
[1] ランドルフ・メーコン・カレッジのジョン・トバーン博士の提供によるものです。
[2] https://pubchem.ncbi.nlm.nih.gov/compound/Tetra_p-bromophenyl_porphyrin
[3] John Thoburn, PhD, Randolph-Macon College からの書面による許可を得て使用されたデータ。
元の記事;
https://www.biotage.com/blog/when-should-i-use-an-amine-bonded-silica-for-flash-chromatography
日本語化:2021年11月
修正:2024年9月