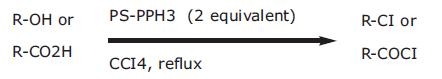|
テクニカルノート PS-Triphenylphosphine
(ウィッティヒ、光延反応、ハロゲン化アルキル除去)
|
 |
【ケミカルデータ】
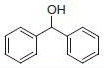
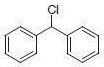
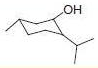
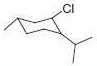
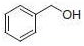
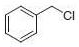
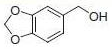
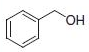
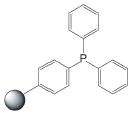
PS-Triphenylphosphineは、トリフェニルホスフィンのレジン担持等価体であるジフェニルホスフィン化ポリスチレンレジンです。レジンの容量はDMF(GC、内部標準法)における臭化ベンジル吸収量の定量によって測定します。本レジンは四塩化炭素中でアルコールまたはカルボン酸を対応する塩化物または酸塩化物に容易に変換することができます(反応式.1)1-3)。反応条件は比較的温和で、生成物は高収率高純度で形成されます(表.1)。
反応式.1 PS-Triphenylphosphineを用いた塩素化 反応式.2 PS-Triphenylphosphineを用いた光延反応
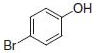
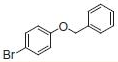
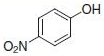
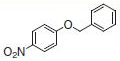
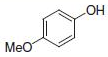
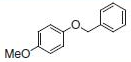
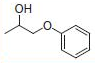
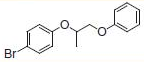
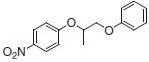
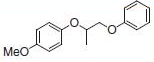
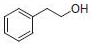
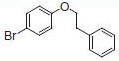
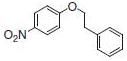
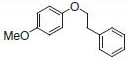
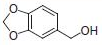
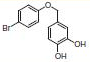
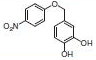
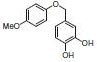
PS-Triphenylphosphineは光延反応でも使用でき、アリルエーテルが良好~優れた収率および高純度で調製されます(反応式.2)4)ここに述べる手順では、面倒なシリカゲル・クロマトグラフィーを行う必要なく高純度の生成物が得られます。過剰なフェノールはMP-Carbonateで除去できます。また、過剰なDBAD (di-tert-butyl azodicarboxylate)ベースのヒドラジド副生成物は、TFAを加え、続いてシリカSPEカートリッジ5)で分離するか、または液液抽出(LLE)を行うことにより除去できます。反応は室温で実施できます。比較研究の結果、過去の推奨事項に反し、窒素による反応混合物のガス除去に大きなメリットはないことが示唆されます6)。しかしながら、担体を加える順序は副生成物を最小限に抑えるうえで重大な意味を持ちます。
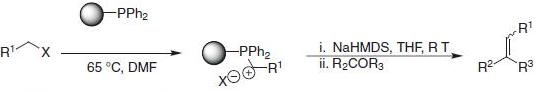
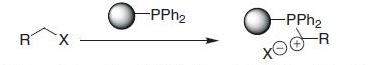
PS-Triphenylphosphineレジンは、ウィッティヒ反応でオレフィンを合成するためや(反応式.3)7、8)、ハロゲン化アルキルのスカベンジャーとして(反応式.4)使用することもできます。
【一般的な実験手順】 ●塩素化(表.1、項目4)
表.1 PS-Triphenylphosphineを用いた酸やアルコールの塩素化
*¹ GC 分析: HP-5 フェニルメチルシリコーンカラム 100-250 ℃, 15 ℃/min, 10 min 保持 *² 未単離 *³ 立体障害のある脂肪族第二級アルコールでは反応が遅く、還流下で3時間後の転換率は28%、16時間後で64%の転換率でした。 同定は 1H NMR
●光延反応(表.2、項目3)
表.2 PS-Triphenylphosphine を用いた光延反応
* 転換率 100%。生成物は加水分解されたアセタール保護基と加水分解されていないアセタール保護基の混合物から成っていました。 生成物は水性塩基およびMTBEを利用し液液抽出で精製できます。
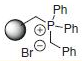
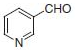
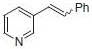
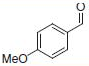
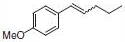
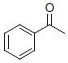
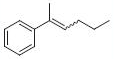
●ウィッティヒ反応(表.3、項目2)
反応式.3 PS-Triphenylphosphineを用いたウィッティヒ反応
表.3 PS-Triphenylphosphineを用いたウィッティヒ反応
*¹ 比率は 1H NMR で決定
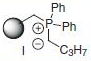
●ハロゲン化アルキルの除去(表.4、項目2)
反応式.4 PS-Triphenylphosphineを用いたアルキルハライドの除去
表.4 PS-Triphenylphosphine (3.0 当量)を用いたアルキルハライドの除去
* GC 分析: HP-5 フェニルメチルシリコーンカラム 100-250℃、 15℃/min、 10min 保持
|
【参考文献】
-
Relles, H. M.; Schluenz, R.W. J. Am. Chem. Soc. 1974, 96, 6469.
-
Regen, S. L.; Lee, D. P. J. Org. Chem. 1975, 40, 1669.
-
Landi, J. J. Jr.; Brinkman, H. R. Synthesis 1992, 1093.
-
Tunoori, A. R.; Dutta, D.; Georg, G. I. Tetrahedron Lett. 1998, 39, 8951.
-
Part Number 440-0200-C.
-
Vasudevan, A.; Park, D. C.; Wodka, D.; Gentles, R. G. J. Comb. Chem. 2002, 4, 442.
-
Bernard, M.; Ford, W.T. J. Org. Chem. 1983, 48, 326.
-
Bolli, M. H.; Ley, S.V. J. Chem. Soc., Perkin Trans. 1. 1998, 15, 2243.
-
Part Number 440-0100-C. Compatible Solvents: DMF (3.5 mL/g), THF (4.1 mL/g), DCM (4.9 mL/g), benzene (3.1 mL/g)
|
【製品番号】
|